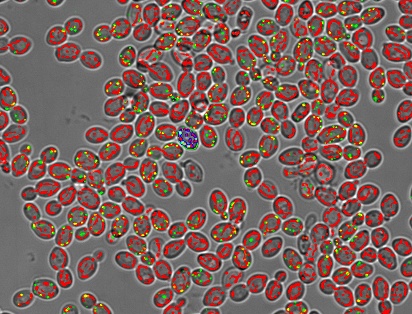
酵母菌高倍显微图像,采用配备转盘共聚焦显微镜和40倍XAPO空气物镜(NA 0.95)的scanR高内涵筛选系统,在微孔板中自动拍摄而成。显微镜原始采集的相机画面尺寸是成像画面的四倍。这些酵母菌直径约为5 μm。图像中红绿信号代表通过scanR软件内置的预训练AI网络生成的细胞器概率分布。
scanR系统正助力研究人员实现前所未有的创造、发现与突破。
在Evident,创新不仅是开发新工具,更是为了构建一个让科学家和临床工作者能够突破界限、揭示未知、在健康、生物和科技领域取得实质性进展的未来。
我们最新升级的scanR 3.6版高内涵筛选系统,正是这一使命的前沿践行者。为深入了解,我们对Evident应用专家、scanR最新版本研发核心成员之—Manoel Veiga博士进行了专访。
随后,我们展开了一场关于未来成像技术、人工智能与规模化科学发现的广泛而深刻的对话。
构建推动科学发现边界的研究平台
问:Manoel,让我们从基础问题开始。在scanR 3.6版本中,“创造”具体指什么?
Veiga博士:在Evident,“创造”意味着为研究人员提供一个超越图像采集的平台—这关乎着促进真知灼见的产生。无论是从头开发全新检测方案,还是创建改进现有检测方案的AI模型,scanR始终扮演着科学创新的强力助推器。
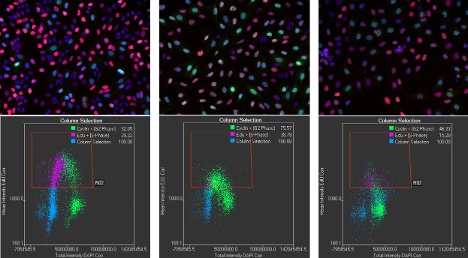
请允许我通过几个新旧案例具体说明。十多年前,受到scanR图像细胞计量界面的启发,研究人员开发了一套名为“定量图像细胞计量”的完整采集分析流程。这项创新催生了多篇癌症研究领域的高影响力论文。1通过绘制数千个单细胞核的DNA含量与特定蛋白标记物的散点图,科学家成功解析了药物反应相关的生物机制与通路。
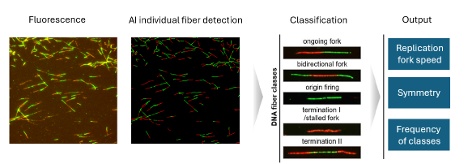
而在2025年的最新案例中,一位研究人员利用scanR的AI与细胞计量功能,开发出名为“基于AI的定量DNA纤维分析流程”的新方法。该工作流程通过自动检测显微镜成像的单个DNA纤维,实现了复制应激反应的自动化研究。2虽然DNA纤维分析技术本身早已存在,但传统方法完全依赖人工图像采集与分析,不仅耗时耗力,还容易受到操作者主观偏差的影响。这项基于AI的定量DNA纤维分析(qAID)新流程,可在数十分钟内完成数千条DNA纤维的成像与多参数分析。
这些案例证明,当研究人员引入scanR系统时,他们获得的远不止是一台显微镜,更是实实在在的科研成果。
问:scanR 3.6版本与前代相比有哪些突破性改进?
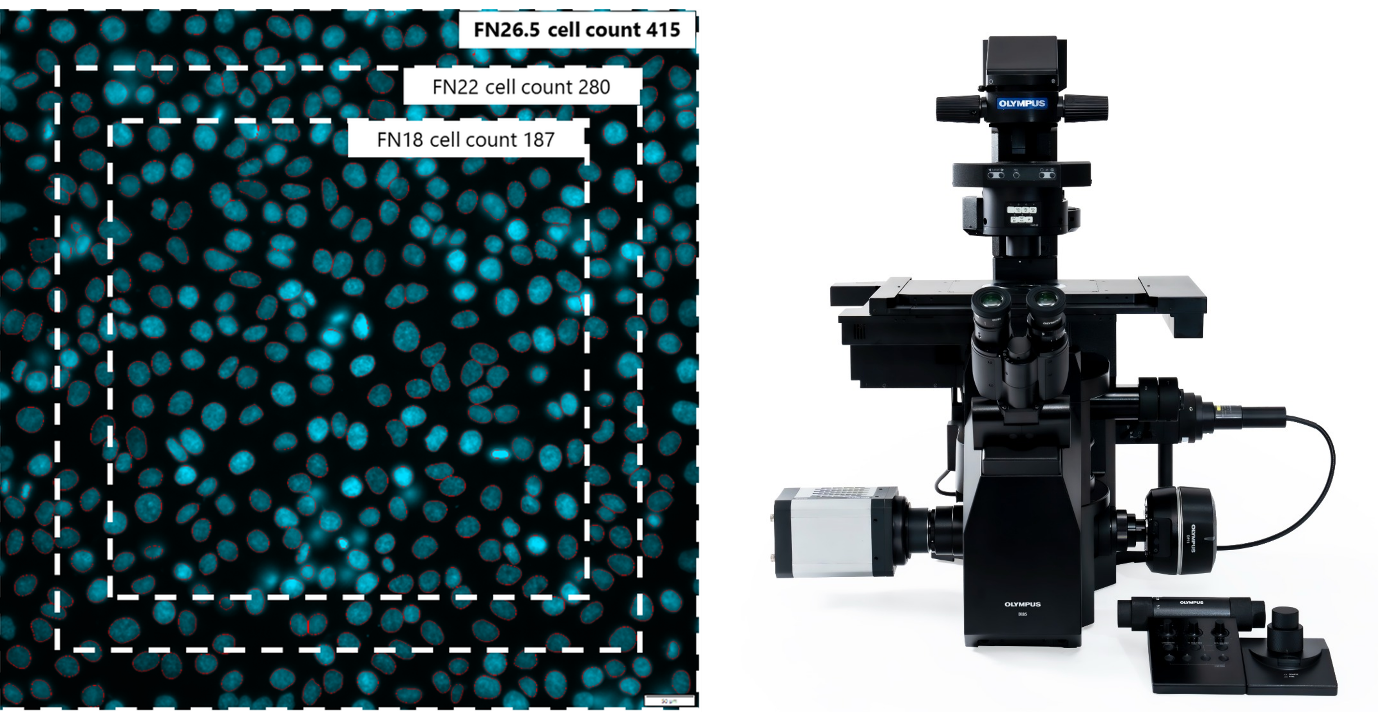
Veiga博士:最重大的升级在于scanR 3.6现在可与IXplore IX85平台联用—该平台配备电动倒置显微镜,拥有行业领先的26.5毫米视场数,提供无与伦比的观测视野。单帧图像尺寸的增大还带来了两大优势:每张图像可捕获的细胞数量增加50%;由于达到相同细胞统计量所需采集的图像数量减少,扫描速度显著提升。
除IX85新平台外,我们现支持更丰富的转盘共聚焦配置。除支持超分辨成像的Yokogawa CSU-W1(SoRa版)外,新增集成Crest X-Light V3转盘,其特殊耦合设计可充分发挥IX85的大视野优势。
需要强调的是,提升实验效率并非仅依赖硬件革新。
软件工作流程同样关键:
- 1.若用户耗费大量时间设置采集参数,再优异的硬件也无法提速。scanR系统仅需软件内点击数次即可启动采集实验,且能全程保持所有细胞清晰对焦。
- 通过并行采集与分析技术,系统整体速度得到显著提升。根据用户反馈,以往需要数周甚至数月才能完成的分析任务,现在可以大幅缩短至数小时即可完成。
问:AI在scanR 3.6版本中似乎发挥着更重要的作用。它是如何增强系统性能的?
Veiga博士:大多数分析检测都遵循相同的工作流程:
1) 对象分割。
2) 提取这些对象的特征。
3) 根据提取的特征对单个细胞进行分类。
4) 并获得每种细胞类型相对于治疗的准确人口百分比。
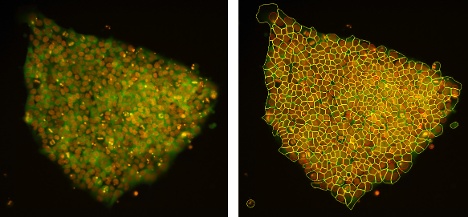
对象分割越精准,分析结果越可靠。原因是系统可精确提取强度与形状因子,从而使后续细胞分类结果更具可靠性。因此,精准的目标分割能力可支持多种成像应用的定制化分析流程。
在过去,用户需要大量的图像处理经验,才能有选择性地仅分割感兴趣的特定结构幸运的是,基于AI技术的智能分割现已大幅简化检测流程。scanR 3.6版附带了五个预训练网络—细胞核、细胞、斑点、结构和透射光下的细胞核—帮助用户完成最常见的分析任务。
除预设模型外,用户无需编程基础即可通过AI训练模块开发特定结构的分割算法无论是识别有丝分裂中的染色体桥、分析延时摄影中的细胞互动,还是鉴定细胞内特定荧光分布模式,AI都能实现传统方法难以企及的精准分析。
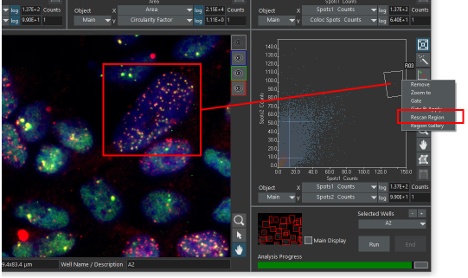
最终,通过区域重扫描功能,scanR的分类与AI工具可快速定位目标细胞或结构并进行高分辨率复拍。
揭示不可见的世界:让隐形变为可见
问:Evident致力于“揭示不可见的世界”以拓展科学发现的边界。这对使用scanR的研究人员意味着什么?
Veiga博士:“揭示不可见的世界”的核心在于揭示传统成像技术难以捕捉的生物系统复杂性。数十年来,显微观察仅局限于显而易见的目标—明亮的特征、表征细胞和荧光标记。然而,scanR系统的深层价值远不止于此。它使研究人员能够捕获并分析数百万个细胞,提供生物变异性的全景视图,而不仅限于少数代表性图像。
更具突破性的是,ScanR系统还能识别亚细胞结构、细胞表型或动态行为,否则这些结构、表型或动态行为就会因过于细微而无法观察,或因过于复杂而无法测量。正因为如此,研究人员才能探索以前无法触及的新科学问题。
这不仅关乎原始数据,更在于揭示前所未见的奥秘。这正是scanR的核心价值:揭示不可见的世界,并为研究人员提供了突破性发现的工具。
问:能否分享一个实际研究案例?
Veiga博士:当然。例如,两张相邻的图像可能在人眼看来极为相似—即使每张图像都包含数千个细胞。然而,当细胞经过分类并以多维直方图呈现时,样本间的差异便会从这些分布图中清晰显现。
由于scanR可以在采集的同时分析数据,所以这意味着我们可以在演示过程中深入了解客户的样本。习惯于较低成像吞吐量和细胞统计数据的研究人员在查看2D直方图时有时会感到惊讶,因为他们发现了意料之外的表型特征。
这些现象的发生概率或许极低,但在2D直方图中会作为显著异常值清晰呈现。尽管比例很低,但如果可重复,它们可能具有生物学相关性。用户可以直接单击2D直方图,查看任何数据点后面的单元格,从而可以完全控制实验,并开始探索新的科学问题。
实现核心价值:满足现实世界的需求
问:scanR 3.6版本在现实世界的可用性方面有什么不同?
Veiga博士:在现实世界中,时间、资源和灵活性都是有限的,因此scanR 3.6在这些限制范围内工作至关重要。我们将scanR设计为模块化,使实验室能够从基本设置开始,并随着需求的发展而扩大规模—无论这意味着增加AI功能、活细胞培养、细胞跟踪分析还是超分辨率成像。此外,scanR和cellSens软件可以在同一台显微镜上共存,从而扩展了系统的灵活性。其核心在于提供一个能满足实验室需求的系统,同时避免不必要的复杂性。
在分析软件方面,scanR自初代版本便展现的精妙设计理念令我深感赞叹。多年来,它的结构使我们能够将新功能无缝集成到分析工具集中,如图像处理、对象分层、细胞跟踪和AI驱动的分割。原始数据永不修改,可在同一数据集上运行多项分析,而无需复制图像。一个或多个AI模型可用于完整Z堆栈或单个Z层中的一个或多个通道。可以对AI概率进行检查,以进行质量控制等。在我看来,这套界面堪称AI分析和检测开发的理想之选。更令人欣喜的是其操作体验—这无疑是我科研生涯中用过最令人愉悦的研究工具!
此外,成像平台管理者们还表示,就使用时间而言,scanR和cellSens软件很快成为他们常用的显微镜解决方案,甚至超过了共聚焦显微镜。他们所取得的成果是衡量成功的真正标准。3
问:最后,最令您期待的是scanR系统在生命科学领域的哪些未来发展方向?以及Evident将如何引领这些变革?
Veiga博士:就我个人而言,最令我期待的是意识到scanR用户不仅是我们的客户,也是我们的密切合作者。他们对系统的反馈意见有助于我们每年对系统进行改进,我们也会尽可能根据他们的科学需求对系统进行调整。此外,ScanR不局限于成像和分析,我们还为建立分析检测提供支持,让我们深入了解他们的研究和显微镜的最新趋势。从公司的角度来看,scanR是让我们在科学方面保持前沿性的重要资产。
最后,在Evident,我们不仅在构建尖端的显微镜解决方案,我们还在为科学的未来做出贡献。而scanR系统,正是这一未来的核心所在。我们的使命是增强研究人员的能力。我们希望每位科学家都能拥有先进的成像工具,无论他们的实验室规模大小或研究问题如何。
关于受访者

Manoel Veiga在西班牙圣地亚哥德孔波斯特拉大学获得了物理化学博士学位。在马德里康普顿斯大学和明斯特大学完成两段博士后研究后,他致力于为全球从事荧光寿命成像显微镜(FLIM)和时间分辨光谱领域的专业人士提供技术支持。他于2017年加入EVIDENT欧洲技术中心,担任全球应用专家,专注于高内涵分析和深度学习技术的开发与应用。
参考文献
- Toledo, L.I., M. Altmeyer, M.B. Rask, C. Lukas, D.H. Larsen, L.K. Povlsen, S. Bekker-Jensen, N. Mailand, J. Bartek, and J. Lukas. 2013. "ATR Prohibits Replication Catastrophe by Preventing Global Exhaustion of RPA." Cell 155 (5): 1088–103.
Michelena, J., A. Lezaja, F. Teloni, T. Schmid, R. Imhof, and M. Altmeyer. 2018. "Analysis of PARP Inhibitor Toxicity by Multidimensional Fluorescence Microscopy Reveals Mechanisms of Sensitivity and Resistance." Nature Communications 9 (1): 2678.
Zonderland, G., R. Vanzo, S.A. Gadi, E. Martín-Doncel, F. Coscia, A. Mund, M. Lerdrup, J. Benada, D. Boos, and L. Toledo. 2022. "The TRESLIN-MTBP Complex Couples Completion of DNA Replication with S/G2 Transition." Molecular Cell 82 (18): 3350–65.e7. - Fagherazzi, Paolo, Timo Diekmann, Alessandra Ardizzoia, Zuzana Machacova, Simran Negi, Anoop Kumar Yadav, Pavel Moudry, Vincenzo Costanzo, and Hana Polasek-Sedlackova. 2025. "Quantitative AI-Based DNA Fiber Workflow to Study Replication Stress." bioRxiv.
- Veiga, Manoel. 2022. "Multimodal Solution Supports Whole Slide Scanning and High-Content Screening in Neuroscience." EvidentScientific.com. 访问日期:2025年7月24日。