FV3000近红外方案助力验证新型近红外二区荧光探针肿瘤特异性靶向
1. 近红外荧光 /光声双模态成像小知识
在众多的生物医学成像技术中,荧光成像(Fluorescence imaging,FLI)由于具有时空分辨率高、检测灵敏度高、响应速度快、可操作性好等优点,已被广泛应用于从临床前到临床的各种生物医学成像技术中。其中,近红外(Near Infrared,NIR)成像由于具有穿透深、光毒性小、组织自发光干扰小等优点,成为现今医学研究尤其是肿瘤诊疗的热点。与传统的荧光标记物如荧光蛋白、染料相比,荧光纳米探针不但可以通过调节化学组成及形貌尺寸轻松实现近红外激发成像,还可通过修饰进一步加载识别、载药及多模态检测等功能。因此迄今为止,研究者们已经探索了大量的荧光探针,以满足日益增长的需求,为精确的疾病诊断和治疗提供新的机会。然而,大多数传统荧光探针的发射在可见光和第一近红外区(NIR-I)(400-1000 nm),由于组织穿透深度浅和空间分辨率低等不足,大大限制了其在生物医学成像中的应用。最近的研究显示荧光成像已可以扩展到第二近红外区(NIR-II, 1000-1700nm),并由于其成像的低光散射和低自身荧光等特性,在深层组织可视化方面表现出巨大的潜力,例如高灵敏度和清晰度,可提供传统荧光成像无法轻易揭示的活体关键信息。
尽管近年来荧光成像技术不断发展创新,但仅仅通过单一模态的光学成像方法仍然很难完美适应目前对活体、深层、超灵敏、三维、高时空分辨率等检测的需求,因此对新型多模态光学检测体系的开发需求日益迫切。光声成像(Photoacoustic imaging, PAI)是近年来发展起来的一种无损的新型生物医学成像方法。当脉冲激光照射到生物组织中时,生物组织产生的超声信号携带了组织的光吸收特征信息,通过探测光声信号能重建出组织中的三维光吸收分布图像来精确描述病变组织的大小、形状、位置和边界。因此,将NIR-II FLI 和 NIR-I PAI结合的双模态成像,利用各自的优势,相互补偿,可有效提高成像精准度,在高效诊断方面具有很大的应用前景。
为了实现高质量的成像效果,探针的设计就显得尤为重要。供体-受体-供体(D-A-D)结构的小分子,由于其优异的生物相容性、明确的化学结构和可定制的光学特性,已成为NIR-II 分子设计的热点。为了获得NIR-II 发射,强缺电子单元,苯并[1,2-c:4,5-c']双([1,2,5]噻二唑)(BBTD)被更广泛地用作受体(图 1a)。由于存在强烈的分子内电荷转移(ICT)效应,荧光分子在水相中的量子产率(QYs)普遍偏低。目前,已经发展了许多提升QYs 的策略,包括与蛋白质疏水结构的染料结合、构建具有聚集诱导发射特性的荧光团、在分子结构中引入屏蔽单元、设计抗猝灭分子等。然而,由于其固有的 ICT 效应,大多数报道的 D-A-D 结构的NIR-II 荧光分子的QYs 仍然相对较低。此外,BBTD 对合成条件要求比较苛刻,限制了通过功能化来发展更先进的 NIR-II 荧光分子。因此,对新的受体单元的探索对于为NIR-II 荧光分子的广泛应用,提供更多的可替代设计策略具有重要意义。
而在检测方面,近红外多模态探针的体外/在体检测也给成像仪器提出了新的挑战。与常规共聚焦成像相比,近红外荧光探针成像需满足以下技术要求:
1. 常规共聚焦显微镜的激发波长大多在 400-650nm 之间,而近红外成像需要>700nm 波长的近红外激光器。
2. 常规成像光路部件如扫描振镜、物镜、光栅等大都只在可见光范围进行增透/校准,无法保证近红外成像效率及准确度。
3. 近红外检测需要>750nm 近红外专用检测器,而普通检测器在近红外区检测效率极低。
此外,对于近红外多模态探针,除了常规的成像检测需求,如果可以将共聚焦扫描成像的信号与其他模态的检测信号进一步联用同步起来,则可以起到强强联合、事半功倍的效果,有助于我们以更精确的时空信号实现对样品的多模态检测成像。
近日,南方科技大学李凯课题组携手南京工业大学刘杰课题组和中国科学院上海药物研究所陈浩课题组提出的受体工程的分子设计策略,可以获得具有高吸光系数和量子产率的NIR-II 荧光探针,从而实现了功能化探针在二维和三维模式条件下实现对肿瘤的靶向检测。
研究结果于2021 年11 月10 日,在 Journal of Materials Chemistry B 上在线发表了题为“Acceptor Engineering of Small Molecule Fluorophores for NIR-II Fluorescent and Photoacoustic Imaging”的研究论文。
此次奥林巴斯生命科学,特邀该论文的第一作者之一李迓曦博士研究生,为我们分享解读主要发现和研究体会。
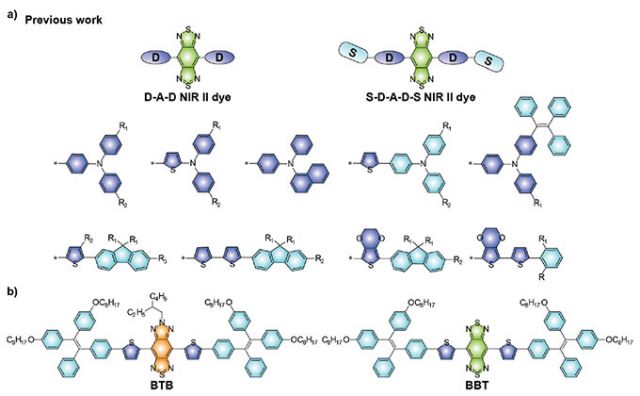
图1. (a)近期报道的基于 BBTD 受体的代表性D-A-D 型NIR-II 荧光分子。(b)本文所报道的新型NIR-II 荧光分子BTB 及对照分子BBT。
2. 本课题研究在成像中的优势有哪些?
传统的荧光探针自身对肿瘤不具备靶向功能,在活体成像中往往是通过实体瘤的高通透性和滞留效应(enhanced permeability and retention effect, EPR 效应)来实现探针在肿瘤部位富集。然而这种被动富集方式对纳米颗粒的尺寸有一定的要求而且往往效率很低。因此,为了增加荧光探针在肿瘤部位的富集,提升成像的效果实现在活体内的高精确诊断,我们利用Arg-Gly-Asp(RGD)靶向肽修饰了纳米探针表面,得到了 BTB-RGD NPs 纳米探针。如图2a 所示,小鼠注射BTB-RGD NPs 48 小时后,肿瘤部位的 NIR-II 荧光信号明显增加,达到最大值;而注射了不具备靶向能力的 BTB NPs 的对照组小鼠,肿瘤部位的荧光信号只有微弱的增加。通过量化分析图 2b 所示, 注射 BTB-RGD NPs 小鼠的肿瘤部位信号在全部时段均高于对照组。在注射后 48 小时,BTB-RGD NPs 组的肿瘤部位的平均信噪比(T/NT)可达到14.1,而相应的对照组仅为 5.0。除荧光成像外,我们还采用光声断层扫描(PAT)进一步证实BTB-RGD NPs 对肿瘤部位的整体靶向作用(图2c)。注射BTB-RGD NPs 小鼠的肿瘤部位的光声信号强度也高于对照组处理小鼠,与 NIR-II 荧光成像结果一致。这些成像结果成功地证明了我们所设计的荧光探针在双模生物成像中的具有很强的应用潜力。一方面,利用 NIR-II 荧光成像的高灵敏度,成功实现了肿瘤边缘二维成像清晰可见。另一方面,与荧光成像相比,PAT 的时间分辨率和灵敏度相对较低,但可以提供优越的空间分辨率和三维可视化。这将有利于肿瘤组织体积图像的重建,在临床转化应用中具有很高的价值。例如,医生可以对肿瘤组织的三维体积信息进行评估,在单剂量造影剂的引导下进行荧光成像手术切除肿瘤。因此,使用单一造影剂整合这两种成像方式为精确的血管成像和癌症治疗提供了巨大的机会。
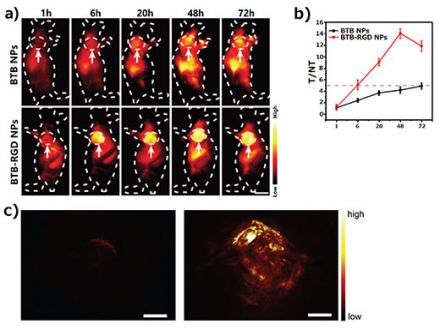
图2.(a)在808 nm 激光(140 mW cm-2)激发下,注射BTB-RGD NPs 或BTB NPs 后 143B肿瘤小鼠进行72 小时拍摄的代表性NIR-II 荧光成像图; (滤光片:1000nm 长通。箭头表示皮下肿瘤。每组小鼠只数(n)= 4。比例尺 = 5 mm。(b)143B 肿瘤成像 72 小时的 T/NT 比值。数据绘制为平均值±SD,n = 4。(c)注射BTB(左)或BTB- RGD NPs(右)48 小时后,小鼠143B 肿瘤的三维光声图像(730 nm 激发)。比例尺 = 2 mm。
3. 在课题的推进过程中,遇到了那些显微成像技术困难?如何解决的?
为了证明BTB-RGD NPs 的靶向能力,首先我们需要通过细胞实验确定其对肿瘤细胞的靶向能力。这就需要借助于共聚焦显微镜开展相关工作,然而当前市售可用的共聚焦显微镜配置的激光器还仅限于可见光区。因此课题组前期为了验证 NIR-II 靶向探针只能借助相似结构可见光区探针替代的方式来间接的证明靶向能力。但这种方式一方面不能直观的证明NIR-II 探针自身的靶向能力,另一方面在实验过程中会增加探针制备的工作量。因此,配有近红外激光的共聚焦显微镜就显得尤为重要。我们就以上要求跟奥林巴斯公司技术团队进行了充分的沟通,获得了奥林巴斯的大力支持,为我们提供了奥林巴斯共聚焦激光扫描显微镜(FV3000)解决这一困难,我们成功确定了BTB-RGD NPs 对肿瘤细胞的靶向能力。如图 3所示,用40 μg mL-1 BTB- RGD NPs 单独孵育后,癌细胞的荧光信号明显高于BTB NPs 的对照组。与此相反,正常 3T3 细胞经BTB-RGD NPs 孵育后的荧光强度与BTB NPs 处理后的荧光强度差异不大。这些结果说明经RGD 功能化之后的纳米颗粒可以促进其对过表达 αvβ3整合蛋白的肿瘤细胞的特异性靶向。
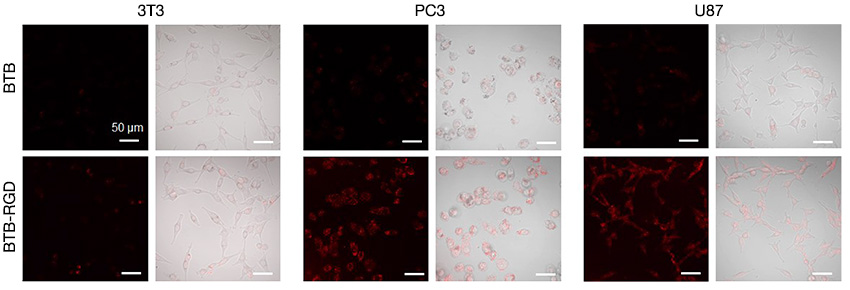
图3. 3T3、PC3 和U87 细胞孵育40 μg mL-1 of BTB-RGD 或 BTB NPs 4 小时后的共聚焦显微成像图。激发波长:730 nm,滤光片:760-890 nm,比例尺 = 50 μm。
针对以上近红外检测需求,奥林巴斯Olympus FV3000 激光共聚焦显微镜提供了成熟系统的近红外成像解决方案,从激光器、光学元件、物镜、检测器各个成像模块多管齐下、全面升级,致力于更高灵敏、更准确多色的近红外成像。而面对多模态探针的检测需求,FV3000还可拓展的ANALOG 单元,可将外部电压信号记录为图像数据与扫描图像同步。还可将扫描时间信号传送到外部设备,通过BNC 端口轻松实现与第三方外部设备的联用,轻松实现荧光信号与电化学信号、FLIM 等多模态检测信号的同步。
FV3000近红外解决方案
此外,随着近年来纳米技术和生命科学研究的飞速发展, 基于荧光纳米探针的生物化学成像应用已取得了许多重要进展。而奥林巴斯作为百年显微镜品牌,一直凭借“光学-数字技术”这一核心竞争力,始终走在行业前沿,以稳定、开放的光学系统,为生命科学、纳米化学、医疗诊断等各个领域提供创新的研究平台及扎实的技术后盾,从纳米探针的光学表征,到其在体深层检测,再到复杂动态过程追踪,我们均可提供灵活多样的解决方案,用百年的深厚积淀,为您的研究征程添油助力。
| FV3000近红外解决方案
|
 | 致谢 本应用说明由以下研究人员协助编写: |
参考文献: 1.V. J. Yao, S. D’Angelo, K. S. Butler, C. Theron, T. L. Smith, S. Marchio, J. G. Gelovani, R. L. Sidman, A. S. Dobraff, C. J. Brinker, A. R. M. Bradbuty, W. Arap. and R. Pasqualini, Ligandtargeted theranostic nanomedicines against cancer, J. Control. Release 2016, 240, 267-286. 2. B. Guo, Z. Sheng, D. Hu, C. Liu, H. Zheng, B. Liu, Through Scalp and Skull NIR-II Photothermal Therapy of Deep Orthotopic Brain Tumors with Precise Photoacoustic Imaging Guidance, Adv. Mater. 2018, 30, 1802591. 3. G. L. Bagnato, N. Irrera, G. Pizzino, D. Santoro, W. N. Roberts, G. Bagnato, G. Pallio, M. Vaccaro, F. Squadrito, A. Saitta, D. Altavilla, and A. Bitto, Dual αvβ3 and αvβ5 blockade attenuates fibrotic and vascular alterations in a murine model of systemic sclerosis, Clin. Sci. 2018, 132, 231-242. 4. N. Zoppi, N. Chiarelli, V. Cinquina, M. Ritelli, and M. Colombi, GLUT10 deficiency leads to oxidative stress and non-canonical αvβ3 integrin-mediated TGFβ signalling associated with extracellular matrix disarray in arterial tortuosity syndrome skin fibroblasts, Hum. Mol. Genet. 2015, 24, 6769-6787. 5. Y. Li, Z. Li, D. Hu, S. Wang, M. Zha, S.-B. Lu, Z. Sheng, and K. Li, Targeted NIR-II emissive nanoprobes for tumor detection in mice and rabbits, Chem. Commun. 2021, 57, 6420-6423.
适于这类应用的产品
Maximum Compare Limit of 5 Items
Please adjust your selection to be no more than 5 items to compare at once
对不起,此内容在您的国家不适用。
